发布时间:2025-04-23 浏览量:0
前言
INTRODUCTION
睡眠不足和慢性炎症,是多种疾病的幕后推手。此前,英国萨里大学发表在《美国国家科学院院刊》上的研究发现,每晚睡眠不足6小时,持续一周,人体就会有7110种基因的功能发生改变,其中涉及到新陈代谢、炎症、免疫力和抗压等功能。
睡眠就像身体的修护模式,帮助修护细胞的损伤、清理大脑代谢废物。睡眠占据了我们生命中约三分之一的时间,但许多人却饱受失眠、呼吸暂停、昼夜节律紊乱等问题的困扰。
健康的睡眠是按时规律的睡眠,入睡时间一般不超过30分钟,有充足的睡眠时间,其中儿童平均每天睡眠时间为10~12小时,青少年为9~10小时,成年人为6~8小时,老年人为5~6小时,不会频繁醒来,不被多梦困扰,醒来后精力充沛,没有嗜睡、乏力、头晕等现象。
失眠则是一种对睡眠时间和质量感到不满足的主观体验。如果经常出现以下情况,那么你可能正在经历失眠:
入睡困难:躺在床上辗转反侧,久久无法入睡;
睡眠维持困难:夜间频繁醒来,难以再次入睡;
早醒:比预期时间提前醒来,无法继续睡眠;
日间功能受损:白天感到疲惫、注意力不集中,甚至情绪低落;
睡眠时间不足:总睡眠时间少于6小时。
失眠不仅影响生活质量,还可能引发焦虑、抑郁,甚至增加心血管疾病和免疫系统疾病的风险。
《每日邮报》曾报道一位46岁的英国女性(Sarah),参加了一个睡眠学校的试验,即连续五天只睡6个小时和每天睡8个小时的容貌对比,结果令所有人大吃一惊。

图中只睡了6小时的皮肤缺乏弹性,皱纹数量上涨了45%,黑斑数量上涨了13%,眼睛变得暗淡无光,整个人看起来老了十几岁
《干细胞研究与治疗》上发表的一项研究综述,作者探讨了睡眠与各种类型干细胞之间的联系。总体来说,这项研究阐述了睡眠障碍与干细胞及外泌体间千丝万缕的联系,也为干细胞临床应用再添理论支撑。

人体内的干细胞(如造血干细胞、间充质干细胞)的增殖、分化、归巢等行为严格受昼夜节律调控,这些活动对于组织再生和稳态至关重要。睡眠的干扰可能会阻碍干细胞的生物行为,从而影响到组织再生以及身体整体的健康状况。
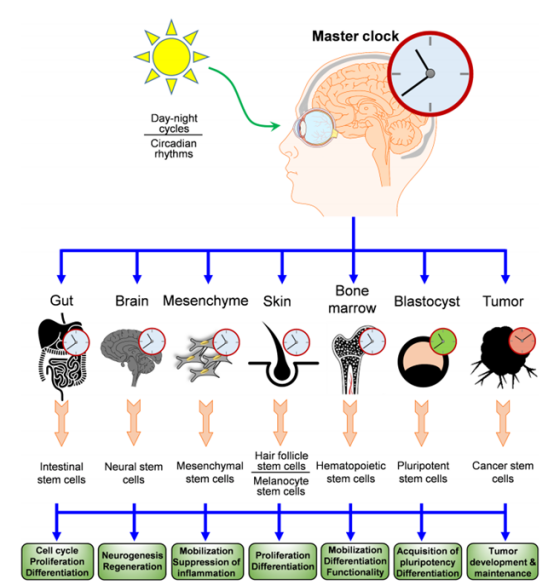
生物钟节律对不同类型干细胞的影响
其中以造血干细胞(HSCs)为例,在夜间通过褪黑素促进自我更新,白天则在肾上腺素驱动下分化为免疫细胞;骨髓中CXCL12基因表达呈现昼夜振荡,调控间充质干细胞(MSCs)迁移。
发表于《Molecular Therapy: Methods & Clinical Development》的一项研究表明,脐带间充质干细胞(hUC-MSCs)外泌体通过调节小鼠的神经炎症和突触功能,在应对睡眠剥夺引起的精神性障碍具有一定的潜力。
该研究表示人脐带间充质干细胞外泌体可显著上调海马区HSP70表达,并通过抑制TLR4/NF-κB通路降低促炎因子(TNF-α、IL-1β)水平,缓解睡眠剥夺小鼠的神经炎症。
(1)可减轻睡眠障碍引起的焦虑行为
作者研究了热休克预处理的人脐带间充质干细胞(hUC- MSCs)衍生的外泌体对小鼠睡眠剥夺引起的焦虑样行为的潜在效果。

结果显示,通过增加行走距离、繁殖次数、在开放臂中花费的时间,以及进入开放臂的条目证实,接受热休克处理的人脐带间充质干细胞外泌体显著减轻了睡眠剥夺引起的焦虑样行为。
(2)可减弱睡眠剥夺引起的认知障碍
此项研究中,研究人员调查了热休克预处理的人脐带间充质干细胞衍生的外泌体对小鼠睡眠剥夺引起的认知障碍的潜在效果。在这个测试中,新臂停留时间和自发交替次数被用作认知功能的指标。

(3)可增加触突关键蛋白的表达
研究人员收集了海马组织进行蛋白质分析,检测了关键突触可塑性相关分子——即突触后密度蛋白95(PSD95)和脑源性神经营养因子(BDNF)的蛋白表达。研究结果表明,用热休克预处理的hUC-MSCs衍生的EVs治疗导致PSD95 (p=0.017)和BDNF(p=0.002)的表达显著增加。

(4)可减轻睡眠剥夺引起的海马区神经炎症
研究人员使用ELISA检测了海马区肿瘤坏死因子α(TNF-α)、白细胞介素-1β(IL-1β)、单核细胞趋化蛋白-1(MCP-1)和白细胞介素-10的蛋白水平。进一步证明其可通过抑制TLR4和p 65的表达,抑制小鼠海马区的剥夺性神经炎症。

良好的睡眠不仅是健康的基础,关于针对睡眠障碍,外泌体现阶段在该方向研究的正向结果,让我们看到在该领域干细胞与外泌体的潜力正逐步被发掘。随着研究的深入,未来干细胞及外泌体科技有望让饱受失眠困扰的人群重获高质量睡眠。未来需要更多的临床试验去推动其进一步的临床发展。我们也期待着技术的早日成熟。
【注】文章内容旨在科普细胞知识,进行学术交流分享,了解行业前沿发展动态,不构成任何应用建议。

