发布时间:2025-12-30 浏览量:0
前言
INTRODUCTION
帕金森是一种神经退行性疾病,其特征是由于黑质中多巴胺能神经元的选择性丧失而引起的运动障碍,又称为“震颤麻痹”。其典型临床表现为静止性震颤、行动迟缓、肌强直姿势步态障碍等。除了常见的运动症状外,帕金森病患者同时还会伴有便秘、嗅觉减退、焦虑抑郁、睡眠障碍、感觉异常等非运动症状。

帕金森病的手抖症状有以下4个特点:
● 静止时明显。
● 精神紧张时加重。
● 做随意动作时减轻。
● 睡眠时消失。
动作迟缓是帕金森病的核心症状:
● 在做起床翻身、刷牙洗脸等日常活动时,动作变得迟缓。
● 缺乏面部表情,不眨眼、双眼凝视,笑容缓慢出现和消失。
● 声调变低,言语不清。
● 写出的字小而弯曲,难以辨读。
帕金森病目前治疗主要以药物治疗为主,辅以康复锻炼,必要时可以考虑手术治疗,主要通过提高脑内纹状体多巴胺水平来达到治疗目的。但是传统的治疗方法无法逆转神经变性,同时也无法增加多巴胺能神经细胞的数目。因此,从病因上寻求一种提高神经细胞数目的治疗方式的突破具有重要意义。
国外一研究团队发表于《Cells》的综述,以帕金森为例系统阐述了MSC-Evs(包含间充质干细胞外泌体)在改善脑部健康,包括改善睡眠及保护神经等方面的作用机制和潜在应用价值。

帕金森病(PD)是一种进行性神经退行性疾病,其特征是大脑黑质致密部内产生多巴胺的神经元逐渐丧失。全球约有超过1000万人患有帕金森病,这种第二大常见的神经退行性疾病正随着人口老龄化而不断增加。传统的药物治疗虽能在早期缓解症状,却难以阻止疾病进展,且长期使用会产生副作用。
近年来,科学家们将目光投向再生医学领域,尤其是MSC-Evs在改善帕金森病等神经退行性疾病方面的潜力。
MSC-Evs是细胞分泌的细胞外囊泡(包含外泌体),携带蛋白质、RNA(特别是miRNA)和脂质等生物活性分子,作为细胞间通信的重要媒介。
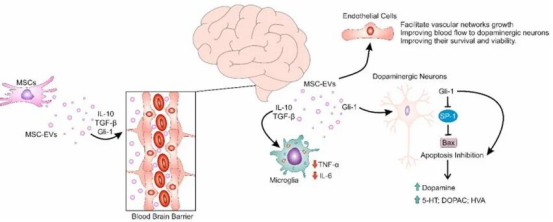
1. 可穿过血脑屏障,并将各种神经营养因子和免疫抑制因子递送至受损多巴胺能神经元,增强其活力和功能。
2. 可减弱小胶质细胞驱动的炎症反应,并预防炎症诱导的多巴胺能神经元损伤。
3. 通过递送IL-10和TGF-β,抑制炎性细胞因子的产生(TNF-α和IL-6),并增加多巴胺、5-羟色胺(5-HT)及其代谢产物的产生。
4. MSC-EVs来源的Gli-1通过抑制特异性蛋白1(SP-1)的激活,增强促凋亡Bax基因的表达,从而抑制多巴胺能神经元的凋亡。
5.通过激活脑内皮细胞中的SMAD 3和p38/MAPK信号通路,促进血管网络的生长,其改善了向受损多巴胺能神经元的血流。
6.携带的多种具有神经保护和免疫调节能力的miRNA,可调节基因表达,防止细胞凋亡,并促进多巴胺能神经元的恢复力。
超过75%的帕金森病患者伴有严重的睡眠障碍,这已成为影响生活质量的主要因素之一。传统安眠药物虽然短期内可改善睡眠,但长期使用会导致依赖性、耐受性,甚至可能加重认知障碍。因此,寻找既能治疗帕金森病核心症状又能改善睡眠的新方法成为当务之急。
研究发现,MSC-Evs可诱导脑和肌肉Arnt样蛋白-1(BMAL 1)和周期昼夜节律调节因子2(PER 2)蛋白的合成增加,其是调节昼夜节律、代谢和受损神经元活力的生物钟的组成部分。
另有动物实验显示,MSC-EVs治疗的PD大鼠的总睡眠时间、慢波睡眠时间和快波睡眠时间延长,这表明MSC-EVs通过恢复昼夜节律相关基因表达来显著改善PD大鼠的睡眠障碍。
间充质干细胞外泌体作为一类具有多重神经保护功能的纳米载体,通过促进血管生成、调节神经炎症、抑制细胞凋亡和氧化应激、增强自噬等多种机制,在脑部健康的临床干预中展现出巨大潜力。

针对帕金森,现有研究中所用到的使用方也较为丰富,如齐鲁细胞公司与上海瑞金医院联合开展的“脐带间充质基质细胞来源外泌体治疗帕金森病的安全性和有效性临床研究”项目中所用到的鼻喷的形式,这种递送方式,相较于传统的口服或注射方式,具有非侵入性、简单易行的特点,更为重要的是它能够直接通过嗅觉神经通路进入大脑,绕过血脑屏障,直接递送到中枢神经系统。
这不仅提高了外泌体的生物利用率,还避免了其在胃肠道和肝脏中的代谢损失。此外,鼻腔施用还具有起效快、副作用小等优点
我们也是期待现有的研究可以早日开花结果,为众多有需求的人带来新的应对策略。
【注】文章内容旨在科普细胞知识,进行学术交流分享,了解行业前沿发展动态,不构成任何应用建议。

