发布时间:2023-08-07 浏览量:0
神经退行性疾病是中枢神经系统(CNS)的致命疾病,其特征是神经系统内特定蛋白质的积累,伴随神经元的逐渐丢失。
但目前为止,其致病机制不完全清晰,神经元变性的不确定原因导致治疗中枢神经系统疾病缺乏有效的治疗手段。其治疗现状面临困境,即便是以改善患者生活质量,延长患者生命为目的的治疗仍然具有挑战性。
干细胞能在体外可分化为上皮细胞和来自神经外胚层的谱系,修复损伤或病变的组织,因此被认为是治疗神经退行性疾病的一种潜在的创新性治疗策略。相比MSC的转分化能力,其旁分泌作用,即通过细胞外囊泡(ev)的释放来改变组织微环境的能力可能对组织修复的贡献更为重要。
MSC治疗的“生力军”——MSC-Ev
细胞外囊泡(EV)是各种细胞释放的膜性小泡,它包裹着干细胞生产的多种蛋白质、RNA、酶类物质,与受损组织进行信息交换或输出,达到改善组织微环境,修复损伤细胞功能的作用。我们都知道,组成人体的器官或组织的基本单位就是细胞,所以,EV的治疗具有从根本上延缓组织功能退化或丧失,起到直接修复组织功能的作用。相比单纯的补充剂或抗炎类药物,这也是我们关注或者更加看重干细胞或其衍生物治疗效果的一个重要原因。
MSCs释放大量具有高治疗能力的Ev,这些Ev装载了繁复的“活性药物”——神经营养因子(NTFs)、免疫调节和抗炎分子,参与神经发生和神经保护的过程,促进神经功能恢复。例如,转化生长因子-β(TGF-β)、白细胞介素-10(IL-10),以及参与神经发育和突触发生的蛋白,如巢蛋白、生长相关蛋白43(GAP-43)和突触素等。大量的神经退行性疾病的神经病理学特征是细胞内或细胞外蛋白原纤维的聚集,导致进行性脑退行性变。
MSC-Ev中的酶类物质,在清除异常蛋白积累和抑制氧化应激方面也起到重要作用。众所周知,阿尔茨海默病(AD)的典型特征是淀粉样蛋白(Aβ)的积累以及神经原纤维缠结、突触和神经元的丢失,导致认知功能的逐渐下降。而Ev中存在高水平的Aβ 降解酶被认为是调节大脑中Aβ 积累水平的有效策略[1]。MSC-Ev中的抗氧化酶,如过氧化氢酶,可以保护海马神经元免受氧化应激和突触损伤[2]。此外,Ev中含有大量的效力miRNA,通过调节神经发生和刺激轴突生长来促进中枢神经系统恢复[3]。
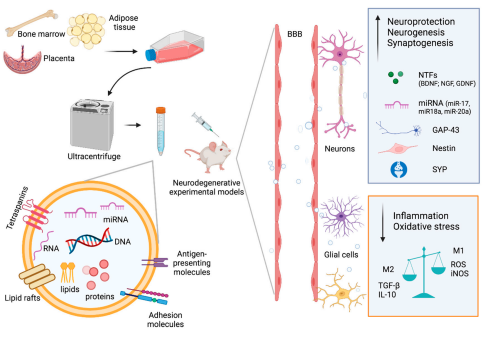
作为神经退行性疾病的创新疗法[4]。
MSC-Ev 的治疗前景
MSC-Ev在一些中枢神经系统疾病,如阿尔茨海默病(AD)、帕金森病(PD)和肌萎缩性侧索硬化症(ALS)等中都表现出良好的治疗潜力。在AD患者中, Aβ的低聚化、过度神经兴奋、神经炎症等都会导致NO的产生,继而发生S-亚硝基化。MSC-Ev在减少氧化损伤和亚硝化损伤方面具有治疗作用。在PD、酒精相关的脑损伤、脑缺血性损伤等模型中,MSC-Ev对包括神经元和胶质细胞在内的多种细胞类型有影响,可以改善线粒体功能障碍引起的氧化应激损伤,对抗神经退行性变。在抗炎功效中,MSC-Ev的治疗,可以增加Foxp3+CD25+调节性T细胞的比例,在AD小鼠模型中诱导了很强的抗炎作用,改善了M2极化的巨噬细胞的数量。
人脐带来源的间充质干细胞中分离出的Ev显著增强了Aβ 降解酶的表达,减少了AD小鼠的Aβ 沉积,减少了神经炎症,提高了小鼠认知能力[5]。XFAD AD小鼠存在血脑屏障的渗漏,而Ev被证明能够启动和修复血脑屏障的渗漏,逆转由AD诱导的血脑屏障的缺陷。不同来源的MSC-Ev能够促进多巴胺能神经元对氧化应激的神经保护,减少黑质多巴胺能神经元的丢失、凋亡,并上调纹状体中的多巴胺水平。在PD大鼠模型中,MSC-Ev治疗可以改善小鼠运动能力。运动神经元(MNs)是肌萎缩性侧索硬化症(ALS)的主要靶点,因为上、下MNs的选择性功能障碍和损伤导致进行性瘫痪和死亡。MSC-EV已经证明能够调节病理SOD1蛋白的聚集,恢复G93A突变的ALS小鼠和MN培养的神经元线粒体蛋白水平。总的来讲,MSC-Ev可以减少氧化应激和亚硝化损伤,作为炎症成分“调节剂”和异常蛋白积累“消除剂”,对抗神经退行性变。
MSC-Ev 的治疗策略
1、如何精准传递至中枢神经病变区域
中枢神经系统疾病治疗的两个关键问题,首当其冲是如何通过血脑屏障(BBB)的通道有效使治疗药物传递至中枢神经系统病变区域。血脑屏障是一种选择性渗透的膜,调节外周血管循环和中枢神经系统之间物质的通道,从而保护中枢神经系统免受有害物质或过度免疫反应的影响,而能够突破BBB是Ev的重要优势。由于其体积小,MSC-Ev能够在输注后有效地迁移到目标器官,而不会被困在肺毛细血管中,穿过血脑屏障,到达大脑中的损伤区域。
另一方面,能够实现无创的治疗新形势,也是Ev的优势,如通过鼻腔给药,跳过胃肠道和肝脏代谢,增加吸收,减少剂量,以达到增效的治疗效果。利用简单有效地设备,如滴剂,气雾剂,喷雾剂等,MSC-Ev可通过嗅球直接进入大脑,进入脑脊液或通过三叉神经途径从鼻上皮到体循环。与其他侵入式给药途径相比,鼻内给药在侵袭性和患者依从性方面占有优势。
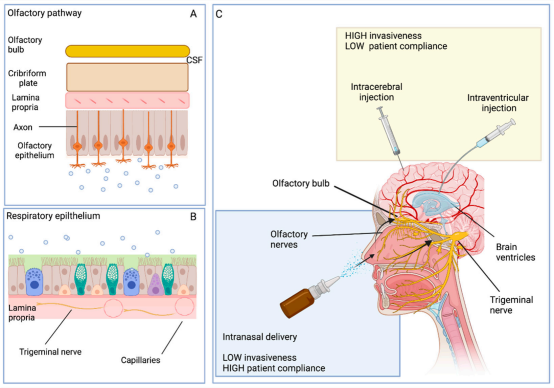
图2. msc-ev的鼻内传递[4]。
2、如何提高药物保留时间
给药浓度、剂量和给药量是影响鼻腔药物进入大脑的重要因素。粘液纤毛清除是鼻内给药动力学的一个限制因素。特别是,细胞色素P450、肽酶和蛋白酶等降解酶的存在可以对药物和细胞成分的代谢产生影响。之所以说MSC-Ev大有可为,不仅仅是其独特的生物学优势,另外,其体外的“可操作性”——创新结合和工程化改造,让人们有更多的思路或者手段探讨提高MSC-Ev治疗效果的策略。
比如在生物技术领域已经通过添加吸收增强剂、粘附聚合物、原位胶凝剂、酶抑制剂和生物活性支架来延长药物在鼻腔内的停留时间,从而获得更高的生物利用度。工程化改造策略包括提高突破BBB的MSC-Ev的数量和浓度,提高特别靶向小胶质细胞和少突胶质细的能力,通过纳米工程提高MSC-Ev的生物利用度,提高EV在体循环中的稳定性等。
【参考文献】
[1] Katsuda, T., et al., Human adipose tissue-derived mesenchymal stem cells secrete functional neprilysin-bound exosomes. Sci Rep, 2013. 3: p. 1197.
[2] de Godoy, M.A., et al., Mesenchymal stem cells and cell-derived extracellular vesicles protect hippocampal neurons from oxidative stress and synapse damage induced by amyloid-β oligomers. J Biol Chem, 2018. 293(6): p. 1957-1975.
[3] Vilaça-Faria, H., A.J. Salgado, and F.G. Teixeira, Mesenchymal Stem Cells-derived Exosomes: A New Possible Therapeutic Strategy for Parkinson's Disease? Cells, 2019. 8(2).
[4]Turano, E., et al., Extracellular Vesicles from Mesenchymal Stem Cells: Towards Novel Therapeutic Strategies for Neurodegenerative Diseases. Int J Mol Sci, 2023. 24(3).
[5]Ding, M., et al., Exosomes Isolated From Human Umbilical Cord Mesenchymal Stem Cells Alleviate Neuroinflammation and Reduce Amyloid-Beta Deposition by Modulating Microglial Activation in Alzheimer's Disease. Neurochem Res, 2018. 43(11): p. 2165-2177.



